Microelectronics • System software
Schwefelsäure / Anodisierbad |

|
This area has not been translated yet. Please stand by. Thank you for your understanding! |
In diesem Artikel erklären wir Ihnen Grundsätzliches zum Anodisierbad und geben Tipps zur Konzentrationsbestimmung und -einstellung.
Während der Schichtbildung laufen im Bad gleichzeitig mehrere Prozesse ab, von denen uns hier nur die beiden wichtigsten interessieren sollen:
Daraus folgt:
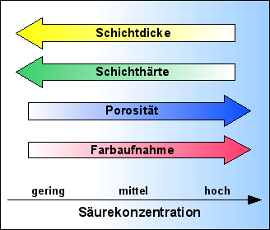
Die Konsequenzen daraus sind:
Ein Hinweis:
Durch Verwendung unseres
Harteloxierzusatzes können auch in Säurebädern höherer
Konzentrationen sehr gute Harteloxalschichten erzeugt werden. Näheres dazu finden Sie in unserer „TM-7 Hartanodisierung“ im Downloadbereich.
Das einfachste, schnellste und am häufigsten angewandte Messverfahren ist die Bestimmung der Dichte des Säurebades mit Hilfe eines Aräometers (Senkwaage). Dabei nutzt man das einfache Prinzip, dass ein Körper so weit in eine Flüssigkeit eintaucht, bis das Gewicht der Verdrängten Flüssigkeit gleich dem Gewicht des Körpers selbst ist. Wenn man den Körper mit entsprechenden Marken versieht, kann an diesen dann direkt die Dichte abgelesen werden.
Üblicherweise werden zugeschmolzene Glasaräometer verwendet, die als Gewicht Bleikügelchen enthalten und entsprechend kalibriert sind. Da die Dichte von Flüssigkeiten immer auch von der Temperatur abhängt, gelten die abgelesenen Werte eines Aräometers immer nur für eine bestimmte Temperatur, die üblicherweise auch auf der Skala angegeben ist.
Je nach der zu messenden Flüssigkeit gibt es Aräometer für verschiedene Dichtebereiche: für leichte Flüssigkeiten wie Alkohol (Dichte etwa 0,79g/cm³, 790g/Liter), die in Wasser gelöst sind, verwendet man dann einen Bereich von 0,79 (reiner Alkohol) bis 1,00 (reines Wasser = 1,00g/cm³) und kann so bestimmen, wie hoch die Konzentration an reinem Alkohol z.B. in Spirituosen ist. Je enger Minimal- und Maximalwert zusammenliegen, desto genauer kann man ablesen, desto schmaler ist aber auch der Bereich, in dem die Senkwaage verwendet werden kann. Man sollte sich überlegen, welche größten oder kleinsten Dichten angenommen werden können und danach das Aräometer wählen - oder man besorgt sich eine Anzahl Senkwaagen mit aufeinander folgenden Messbereichen und kann so sehr exakt messen.
Die Messung mit einem Aräometer ist denkbar einfach: man lässt dieses langsam in die zu messende Flüssigkeit tauchen und liest dann den Wert ab, an dem der Flüssigkeitsspiegel steht. Zu diesem Dichtewert liest man nun einfach den Prozentwert aus der Tabelle ab.
Dies ist eine weitere einfache Methode. Dabei misst man ein genaues Volumen des Anodisierbades ab und ermittelt dessen Masse. Durch die einfache Formel
kann dann die Dichte berechnet und damit über die Tabelle auf die Säurekonzentration geschlossen werden.
Ein Beispiel:
Dem zu prüfenden Anodisierbad werden mit einem Messkolben 50cm³ entnommen und diese gewogen. Mit dem Ergebnis (55,2g) wird nun anhand obiger
Formel die Dichte zu 55,2g/50cm³ = 1,104g/cm³ berechnet. Die Tabelle liefert dann für diese Dichte eine Säurekonzentration von etwas über 15%.
Bitte beachten Sie, dass in die Dichte des Anodisierbades natürlich auch andere Stoffe wie gelöstes Aluminium, Zusätze etc. einfließen und das Ergebnis etwas verfälschen können. Durch die deutlich höhere Konzentration an Schwefelsäure sind die Abweichungen aber meist vernachlässigbar. Für eine genaue Bestimmung des Säuregehaltes muss eine sogenannte Titration durchgeführt werden, wie sie im nächsten Abschnitt ansatzweise beschrieben ist.
Bei der Titration wird die Menge einer unbekannten Säure bestimmt, indem eine Base exakt bekannter Konzentration solange hinzugegeben wird, bis die Lösung neutral reagiert (also den pH-Wert 7 hat). Die Überwachung des pH-Wertes erfolgt dabei entweder mit Hilfe spezieller Farbstoffindikatoren, die durch Farbumschlag die Neutralität der Lösung anzeigen oder (heutzutage vermehrt, da genauer) durch elektronische ph-Messgeräte.
Die Titration ist deutlich genauer als die zuvor beschriebenen Verfahren zur Dichtemessung, da nur die wirklich vorhandene Säure und nicht gelöstes Aluminium etc. ins Messergebnis einfließen.
Der Aufwand ist aber auch deutlich höher und normalerweise unverhältnismäßig, wenn es nur um Auffrischung eines vorhandenen Bades geht.
Deswegen verzichten wir hier auf eine genauere Darstellung des Verfahrens. Bei Interesse lassen sich leicht vielfältige Informationen zu diesem Thema im Internet finden.
Da die im Handel erhältliche Säure oftmals eine andere (=höhere) Konzentration besitzt als benötigt wird, lautet eine wichtige Frage in der Praxis:
„Mit welcher Menge Wasser muss ich Säure der Konzentration X Prozent verdünnen, um Säure der
Konzentration Y Prozent zu erhalten?“
Im Folgenden werden die dazu nötigen einfachen Schritte erklärt und das Ganze an einem anschaulichen Beispiel durchgerechnet.
Benötigt man eine bestimmte Konzentration, so geht man wie folgt vor:

Da sich alle Säuren beim Verdünnen massiv erwärmen, sollten Sie die Säuren langsam in viel kaltes Wasser einrühren, nie umgekehrt! Es besteht sonst Spritz- und Verdampfungsgefahr! Für das obige Verfahren heisst dies, dass wir die in (3.) berechnete Säuremenge
bereits in eine passende Menge (kalten) Wassers einrühren und schließlich nur noch den Rest bis zum gewünschten Endvolumen auffüllen.
Nicht vergessen: Schutzhandschuhe und vor allem Schutzbrille sowie alte Kleidung tragen!
Ein Beispiel: Wir haben 38%ige Batteriesäure zur Verfügung und möchten mit dieser 10 Liter 15%ige Säure
herstellen.
Entsorgungshinweise zu verbrauchten Anodisierbädern finden Sie in unserer „TM-5 Entsorgung von Chemikalien“ im Downloadbereich.
Im Folgenden finden Sie tabellarisch die Konzentrationen von Schwefelsäure. Unter „Bemerkungen“ finden Sie die Bereiche markiert, für die jeweiligen Säurekonzentrationen üblicherweise eingesetzt werden sollten.
| % H2SO4 | Dichte ρ (+20°C) in g/cm³ |
H2SO4 in g/l |
H2SO4 in mol/l |
Bemerkungen |
|---|---|---|---|---|
| 1 | 1,0051 | 10,05 | 0,103 | |
| 2 | 1,0118 | 20,24 | 0,206 | |
| 3 | 1,0184 | 30,55 | 0,312 | |
| 4 | 1,0250 | 41,00 | 0,418 | |
| 5 | 1,0317 | 51,59 | 0,526 | Hartanodisierung ¹ |
| 6 | 1,0385 | 62,31 | 0,635 | |
| 7 | 1,0453 | 73,17 | 0,746 | |
| 8 | 1,0522 | 84,18 | 0,858 | |
| 9 | 1,0591 | 95,32 | 0,972 | |
| 10 | 1,0661 | 106,60 | 1,087 | |
| 11 | 1,0731 | 118,00 | 1,203 | |
| 12 | 1,0802 | 129,60 | 1,321 | Dekorative Anodisierung |
| 13 | 1,0874 | 141,40 | 1,442 | |
| 14 | 1,0947 | 153,30 | 1,563 | |
| 15 | 1,1020 | 165,30 | 1,685 | |
| 16 | 1,1094 | 177,50 | 1,810 | |
| 17 | 1,1168 | 189,90 | 1,936 | |
| 18 | 1,1234 | 202,40 | 2,063 | |
| 19 | 1,1318 | 215,00 | 2,192 | |
| 20 | 1,1394 | 227,90 | 2,324 | |
| 21 | 1,1471 | 240,90 | 2,456 | |
| 22 | 1,1548 | 254,10 | 2,591 | |
| 23 | 1,1626 | 267,40 | 2,726 | |
| 24 | 1,1704 | 280,90 | 2,864 | |
| 25 | 1,1783 | 294,60 | 3,004 | |
| 26 | 1,1862 | 308,40 | 3,144 | |
| 27 | 1,1942 | 322,40 | 3,287 | |
| 28 | 1,2023 | 336,60 | 3,432 | |
| 29 | 1,2104 | 351,00 | 3,579 | |
| 30 | 1,2185 | 365,60 | 3,728 | |
| 31 | 1,2267 | 380,30 | 3,878 | |
| 32 | 1,2349 | 395,20 | 4,029 | |
| 33 | 1,2432 | 410,30 | 4,183 | |
| 34 | 1,2515 | 425,50 | 4,338 | |
| 35 | 1,2599 | 441,00 | 4,496 | |
| 36 | 1,2684 | 456,60 | 4,656 | |
| 37 | 1,2769 | 472,50 | 4,818 | Batteriesäure |
| 38 | 1,2855 | 488,50 | 4,981 | |
| 39 | 1,2941 | 504,70 | 5,146 | |
| 40 | 1,3028 | 521,10 | 5,313 | |
| 41 | 1,3116 | 537,80 | 5,483 | |
| 42 | 1,3205 | 554,60 | 5,655 | |
| 43 | 1,3294 | 571,60 | 5,828 |
¹ Bei Verwendung unseres Harteloxierzusatzes kann auch mit Bädern für dekorative (=farbige) Anodisierungen (12-20% Säuregehalt) harteloxiert werden, so dass Sie nur ein einziges Anodisierbad benötigen.